top of page



Molalidad



La molalidad (m) de un componente es la relación entre el número de moles del soluto respecto a kilogramos (kg) de solvente.

¿Cómo pesar el agua?

En este tipo de soluciones, al solvente lo expresamos en unidades de masa, por lo que debemos usar su densidad.
Experimentalmente pesamos el vaso vacío. Luego, pesamos el vaso con agua y la diferencia es el peso del agua, ambas formas son válidas.


Ejemplo con su procedimiento
Calculemos la molalidad de una disolución formada por treinta gramos de cloruro de sodio (NaCl) en 500 mL de agua.
Paso 1:
Identificamos el soluto y el solvente


Paso 2:
Transformemos a las unidades de la fórmula de molalidad.
Utilizando la densidad del agua.




Paso 3:
Reemplazamos en la fórmula.
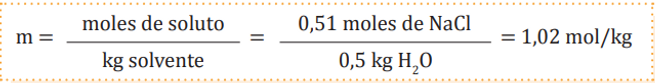
Refuerza tu conocimiento con el siguiente video

Realiza los siguientes ejercicios


bottom of page
